以嶺藥業凈利潤破20億!手握19個獨家產品
近段時間,中藥創新龍頭企業之一以嶺藥業喜訊頻傳:乳結泰膠囊上市許可持有人變更成功,公司再獲一個獨家中成藥;公司首款生物藥1類新藥BIO-008獲批臨床,研發管線再添重磅新品。以嶺藥業以絡病理論為基礎,不斷實現創新突破,近幾年1類新藥研發管線從中成藥拓展至化學藥、生物藥,公司正實現快速成長……截至4月3日收盤,公司總市值超過480億,為A股中藥股TOP6企業。
凈利潤首破20億,獨家中成藥增至19個
2023年1月31日,以嶺藥業發布2022年度業績預告,預計凈利潤為21.5億元至24.2億元,同比增長60%至80%,這是公司上市以來最佳業績。
圖1:近五年以嶺藥業的凈利潤情況(單位:億元)

來源:公司年報、業績預告
目前,以嶺藥業重點布局中醫藥板塊,在創新絡病理論指導下,圍繞心腦血管、呼吸系統、腫瘤、神經系統、泌尿系統等發病率高、市場用藥量大的疾病領域,已擁有多個暢銷獨家中成藥。2023年3月2日,公司發布公告稱,乳結泰膠囊的藥品補充申請獲批,公司成為了該產品上市許可持有人,截至目前以嶺藥業的獨家中成藥升至19個。
表1:以嶺藥業的獨家中成藥情況
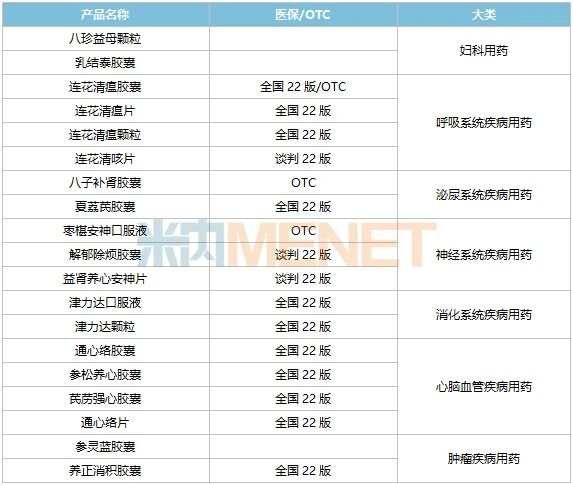
來源:米內網中國上市藥品(MID)數據庫
通心絡膠囊、參松養心膠囊、芪藶強心膠囊是以嶺藥業在心腦血管中成藥領域的“三大王牌”,米內網數據顯示,2021年在中國三大終端六大市場(統計范圍見文末),通心絡膠囊和參松養心膠囊的合計銷售額均超過20億元,而芪藶強心膠囊也在9億元以上,有望在2022年突破10億元關口。
連花清瘟膠囊和連花清瘟顆粒是公司在呼吸系統中成藥領域的“雙子星”,2021年在中國三大終端六大市場的合計銷售額均超過了20億元。
從獲批時間來看,連花清咳片、解郁除煩膠囊、益腎養心安神片是以嶺藥業近幾年獲批的獨家新品。連花清咳片在2020年獲批后立即進入了當年的國家醫保談判目錄,在醫保助力下,該獨家產品2021年在中國三大終端六大市場的合計銷售額已接近2000萬元,銷售有望繼續走高;而2021年獲批的解郁除煩膠囊和益腎養心安神片也在今年年初的醫保談判中順利“入保”,成為2022版國家醫保談判目錄品種,未來有望實現銷售放量。
中藥新藥持續加碼,這個百億市場將迎新突破
以嶺藥業在中藥創新方面堅持開展復方中藥、組分中藥、單體中藥多渠道研發,建立了具有自主知識產權的新藥研發體系,科技創新能力居中藥行業前列。公司表示,未來計劃每年申報1-2個中藥創新藥上市。
表2:以嶺藥業2022年申報的中藥新藥情況
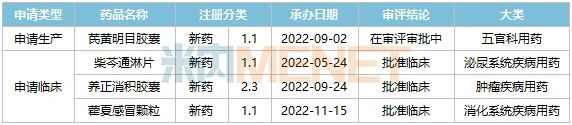
來源:米內網中國申報進度(MED)數據庫
芪黃明目膠囊于2022年申報上市,該新藥用于治療糖尿病視網膜病變。米內網數據顯示,2021年在中國三大終端六大市場,中成藥眼科其它用藥、白內障用藥以及化學藥(含生物藥)眼科用藥合計市場規模接近200億元,目前暫無眼科中藥1類新藥獲批上市,以嶺藥業有望打破這個局面。
此外,公司已上市的津力達顆粒用于2型糖尿病氣陰兩虛證,2021年在中國三大終端六大市場合計銷售額超過1億元。以嶺藥業表示,未來芪黃明目膠囊獲批,可與津力達顆粒發揮協同作用,為糖尿病伴隨視網膜病變的患者提供更多用藥選擇。
2022年,公司再有2個中藥1.1類新藥和1個中藥2.3類新藥獲批臨床,公司的中藥新藥矩陣進一步壯大。
表3:以嶺藥業部分獲批臨床并在II期以上臨床階段的中藥新藥
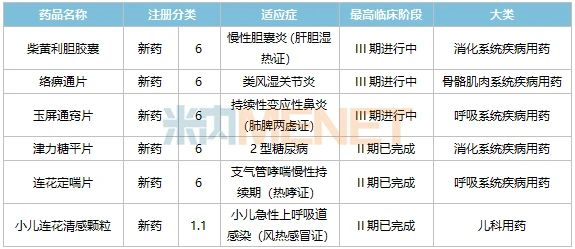
來源:米內網中國臨床試驗數據庫
目前,柴黃利膽膠囊、絡痹通片、玉屏通竅片已進入III期臨床階段,有望成為繼芪黃明目膠囊后申報上市的中藥新藥。以嶺藥業在中藥新藥研發上已做到了合理的梯隊布局,形成了“上市一批、臨床一批、儲備一批”的良性循環,公司的創新實力正在不斷提升。
“化生”1類新藥接踵而至,14個過評產品亮眼
米內網數據顯示,2021年中國三大終端六大市場藥品銷售規模已超過15000億元,在國采與醫保談判雙重推動下,萬億市場風起云涌。
作為中藥創新龍頭企業之一的以嶺藥業,在集中火力加大中藥新藥研發的同時,近幾年公司化學藥與生物藥1類新藥的研發也是碩果累累,公司的市場競爭力不斷提升。
表4:以嶺藥業部分在研的重磅化學藥/生物藥1類新藥情況
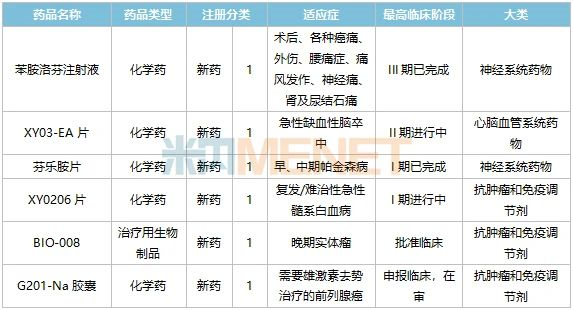
來源:米內網中國申報進度(MED)數據庫
化學藥1類新藥苯胺洛芬注射液由以嶺藥業與廣東中科藥物研究有限公司合作開發,該新藥的發明專利、新藥證書和生產批件等項目成果由以嶺藥業獨家擁有。據悉,該藥屬于非甾體類鎮痛藥,擬用于術后、各種癌痛、外傷、腰痛癥(急性期、慢性惡化期)、痛風發作、神經痛、腎及尿結石痛等。目前,該新藥III期臨床已完成,并正籌備申報上市,有望成為新藥品注冊管理辦法實施以來,以嶺藥業首個獲批上市的化學藥1類新藥。
而公司首個生物藥1類新藥也于近日獲批臨床,據悉BIO-008是靶向Claudin18.2的單克隆抗體,通過抗體和補體依賴介導的細胞毒性作用,誘導細胞凋亡、抑制腫瘤細胞增殖,殺傷Claudin18.2陽性腫瘤細胞。目前,以嶺藥業尚未有生藥物獲批上市,BIO-008獲得臨床試驗批準,標志著公司在生物藥領域首次獲得了階段性的成果。
表5:以嶺藥業已過評/視同過評的產品
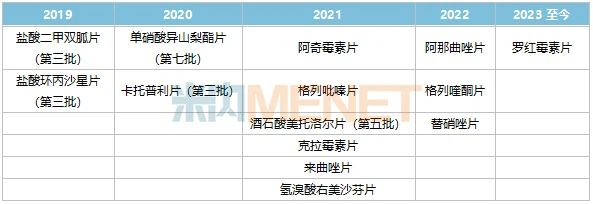
來源:米內網中國申報進度(MED)數據庫
一致性評價與國采是業界大事,截至目前,以嶺藥業已過評/視同過評的產品達14個,其中第三批、第五批、第七批國采合共中標5個產品。
在中國城市公立醫院、縣級公立醫院、城市社區中心及鄉鎮衛生院(簡稱中國公立醫療機構)終端,第三批和第五批國采執行后,以嶺藥業的卡托普利片、鹽酸二甲雙胍片、鹽酸環丙沙星片以及酒石酸美托洛爾片的市場份額均有上漲,其中鹽酸環丙沙星片2022上半年的市場份額已到達40%以上,國采助力不容小覷。
此外,目前以嶺藥業還有兩款重磅仿制藥申報上市在審,塞來昔布膠囊2021年在中國三大終端六大市場合計銷售額超過8億元,而沙庫巴曲纈沙坦鈉片合計銷售額則超過22億元,以嶺藥業按4類仿制申報上市,若順利獲批則視同過評,公司的化學藥產品矩陣越來越強大。
資料來源:公司年報、公告、米內網數據庫
注:米內網《中國三大終端六大市場藥品競爭格局》,統計范圍是:城市公立醫院和縣級公立醫院、城市社區中心和鄉鎮衛生院、城市實體藥店和網上藥店,不含民營醫院、私人診所、村衛生室,不含縣鄉村藥店;上述銷售額以產品在終端的平均零售價計算。統計數據截至4月3日。









