20億抗痛風藥跌落“神壇”!20款重磅1類新藥來襲 發起沖擊
日前,恒瑞醫藥發布公告稱,公司的1類抗痛風新藥SHR4640片獲批臨床,并將于近期開展;隨后中國醫藥其下屬全資子公司天方藥業獲得國家藥監局核準簽發的非布司他片《藥品補充申請批準通知書》,該藥品上市許可持有人由南京海納制藥變更為天方藥業。米內網數據顯示,受集采影響,抗痛風制劑2021年銷售額出現下滑,20億大品種腰斬。據不完全統計,目前有38款抗痛風新藥獲批臨床,其中20款是1類新藥,涉及江蘇恒瑞醫藥、廣東東陽光藥業、江蘇康緣藥業、江蘇先聲藥業、長春金賽藥業等多家企業。
集采沖擊,20億抗痛風藥跌落“神壇”
近年抗痛風制劑市場規模(單位:億元)
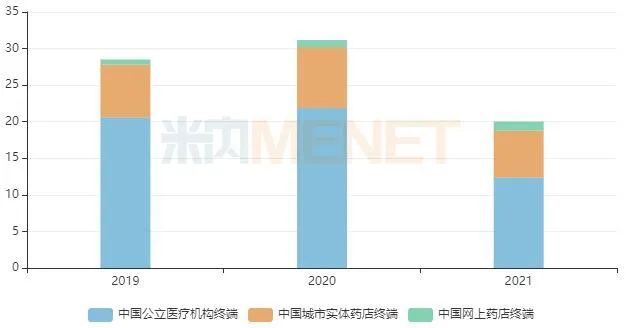
來源:米內網數據庫
米內網數據顯示,近年抗痛風制劑在中國城市公立醫院、縣級公立醫院、城市社區中心及鄉鎮衛生院(簡稱中國公立醫療機構)終端、中國城市實體藥店終端和中國網上藥店終端的銷售額穩步增長,2020年超過30億元,然而受集采影響,2021年銷售額出現下滑,其中,中國公立醫療機構終端下滑幅度最大,超過40%;而中國網上藥店終端同比增長近30%。
2021年抗痛風制劑TOP5產品銷售情況(單位:億元)
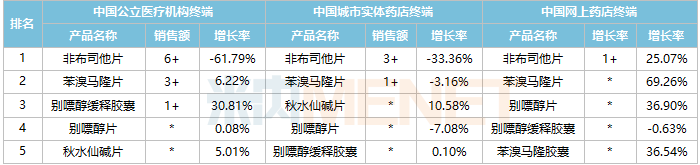
注:銷售額低于1億元用*表示
來源:米內網數據庫
從TOP5產品來看,非布司他片是抗痛風制劑的第一大品種,被納入第三批集采后,銷售額大幅下滑,從2020年頂峰的20億級別下滑至10億級別。其中,中國公立醫療機構終端下滑幅度最大,超過60%。
值得注意的是,非布司他片、苯溴馬隆片、別嘌醇片和苯溴馬隆膠囊在中國網上藥店終端均有雙位數的大幅增長,其中,苯溴馬隆片增速最快,同比增長近70%。
30億抗痛風制劑市場!僅3個產品過評
抗痛風制劑過評情況
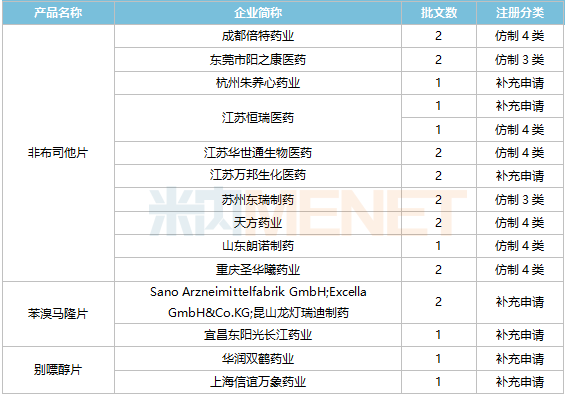
來源:米內網一致性評價數據庫
目前,抗痛風制劑中已有非布司他片、苯溴馬隆片和別嘌醇片3個產品過評,其中,TOP1產品非布司他片是過評“大戶”,江蘇恒瑞醫藥、江蘇萬邦生化醫藥、成都倍特藥業等10家企業均已過評,宜昌人福藥業、華潤雙鶴藥業、浙江華海藥業、浙江諾得藥業等16家企業以新分類報產在審,獲批后將視同過評。
日前,中國醫藥發布公告,其下屬全資子公司天方藥業獲得國家藥監局核準簽發的兩份“非布司他片”《藥品補充申請批準通知書》,該藥品上市許可持有人由南京海納制藥變更為天方藥業。中國醫藥表示,天方藥業成為該藥品的上市許可持有人,進一步豐富公司產品線,有利于提升市場競爭力。截至公告日,天方藥業在該藥品項目累計投入約2085萬元。未來,該產品的市場競爭將會更加激烈。
苯溴馬隆片作為抗痛風制劑暢銷產品之一,僅有3家企業擁有生產批文,其中,2家企業過評,宜昌東陽光長江藥業在2019年拿下該產品首家過評。此外,常州康普藥業的苯溴馬隆片的一致性評價補充申請在審。
超30款抗痛風新藥在研,恒瑞、康緣……1類新藥來襲
近日,恒瑞醫藥發布公告稱,公司SHR4640片收到國家藥監局的《藥物臨床試驗批準通知書》,將于近期開展聯合非布司他片進行痛風患者高尿酸血癥臨床試驗。截至目前,公司在該研發項目上已投入研發費用1.83億元。
據了解,SHR4640片是公司自主創新的1類抗痛風藥物,其陽性對照藥為阿斯利康子公司Ardea Biosciences開發的Lesinurad。Lesinurad于2015年12月獲得美國FDA批準,用于與黃嘌呤氧化酶抑制劑聯用治療黃嘌呤氧化酶抑制劑單藥治療后未實現目標血清尿酸水平的與痛風關聯的高尿酸血癥,劑型為片劑,規格為200mg;2016年2月,Lesinurad獲歐盟批準;2017年8月,Lesinurad和別嘌呤醇的固定劑量組合藥物獲美國FDA批準,商品名Duzallo;目前國內暫無Lesinurad、Duzallo制劑獲批。
部分抗痛風制劑1類新藥獲批臨床情況
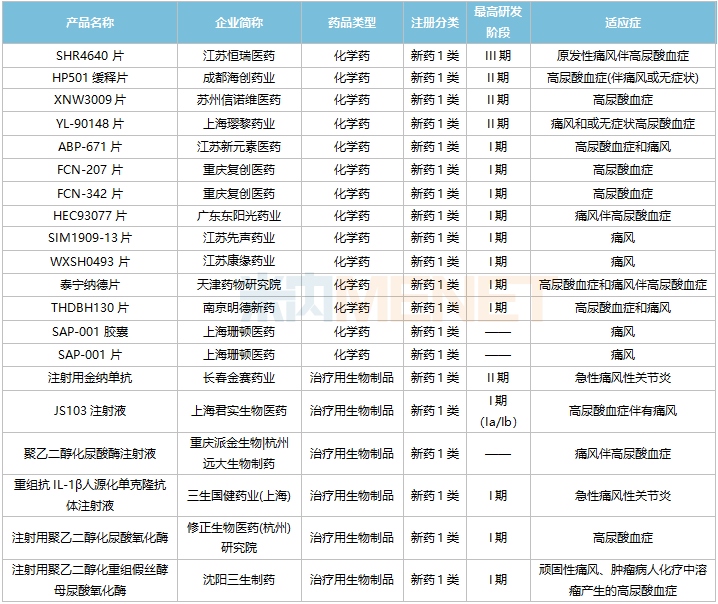
圖片來源:米內網中國藥品臨床試驗公示庫
據不完全統計,目前有38款抗痛風新藥獲批臨床,其中1類新藥有20款,涉及江蘇恒瑞醫藥、廣東東陽光藥業、江蘇康緣藥業、江蘇先聲藥業、長春金賽藥業等多家企業。
恒瑞醫藥的SHR4640片的研發進展最快,已進入III期臨床,有望成為首個獲批的國產1類新藥。此外,成都海創藥業的HP501緩釋片、蘇州信諾維醫藥的XNW3009片、上海瓔黎藥業的YL-90148片、長春金賽藥業的注射用金納單抗均已進入II期臨床階段









